الامتثال لممارسات التصنيع الجيدة (cGMP)

يغطي ممارسات التصنيع الجيدة (GMP) جميع جوانب الإنتاج؛ بدءًا من المواد الخام والمباني والمعدات وصولًا إلى التدريب والنظافة الشخصية للموظفين. تُعد الإجراءات التفصيلية المكتوبة ضرورية لكل عملية قد تؤثر على جودة المنتج النهائي. يجب أن تكون هناك أنظمة توفر دليلًا موثقًا على اتباع الإجراءات الصحيحة باستمرار في كل خطوة من خطوات عملية التصنيع – في كل مرة يتم فيها تصنيع المنتج. وضعت منظمة الصحة العالمية (WHO) إرشادات مفصلة لممارسات التصنيع الجيدة. وقد وضعت العديد من الدول متطلباتها الخاصة لممارسات التصنيع الجيدة بناءً على ممارسات التصنيع الجيدة لمنظمة الصحة العالمية. وقامت دول أخرى بتوحيد متطلباتها.
يجب أن تُضمن الجودة العالية أثناء عملية التصنيع؛ ولا يُمكن اختبارها على المنتج بعد ذلك. تمنع ممارسات التصنيع الجيدة (GMP) الأخطاء التي لا يُمكن تلافيها من خلال مراقبة جودة المنتج النهائي. فبدونها، يستحيل التأكد من أن كل وحدة من الدواء أو الجهاز الطبي تُضاهي جودة وحدات المنتج التي تم اختبارها في المختبر.
إن إنتاج منتجات رديئة الجودة لا يوفر المال. على المدى البعيد، يكون اكتشاف الأخطاء بعد وقوعها أكثر تكلفةً من منعها من البداية. صُممت ممارسات التصنيع الجيدة (GMP) لضمان عدم وقوع الأخطاء. يُعد تطبيق ممارسات التصنيع الجيدة استثمارًا في منتج عالي الجودة، مما يُحسّن صحة المريض والمجتمع، ويعود بالنفع على صناعة الأدوية والعاملين في المجال الصحي. يؤدي إنتاج وتوزيع منتجات رديئة الجودة إلى فقدان المصداقية لدى الجميع: مؤسسات الرعاية الصحية العامة والخاصة، وكذلك لدى الشركة المصنعة.
تحدد قواعد GMP المتطلبات ذات الصلة بالتنظيم والموظفين والمباني والمرافق والمعدات وإدارة المستندات والتصميم والتطوير والمشتريات وإدارة الإنتاج ومراقبة الجودة والمبيعات وخدمات ما بعد البيع والتحكم في المنتجات غير المطابقة ومراقبة الأحداث السلبية والتحليل والتحسين وما إلى ذلك. ويجب على مصنعي الأجهزة الطبية إنشاء نظام إدارة الجودة وتحسينه وفقًا لقواعد GMP هذه.
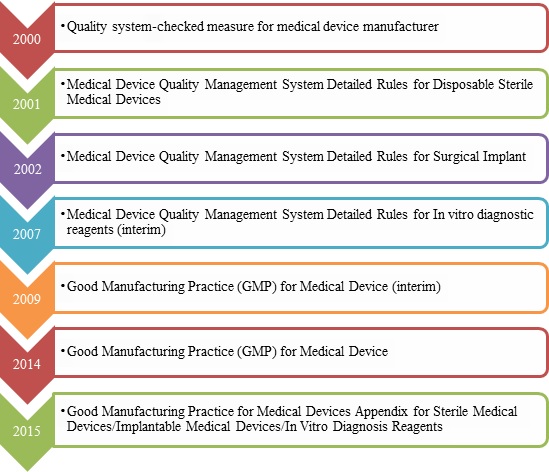
1. سجل مراجعة GMP للأجهزة الطبية
2. النقاط الرئيسية لممارسات التصنيع الجيدة (GMP)
2.1 التنظيم والموظفين
ملاحظة:
يجب على العاملين في مجال الأجهزة الطبية الحيوانية القابلة للزرع والأجهزة الطبية المتماثلة تدريبهم على التقنيات الخاصة، وإجراءات الوقاية والاحتياطات اللازمة، وفقًا لنوع المنتج وطريقة التشغيل. ويشمل ذلك عمال النظافة وموظفي الخدمة، وغيرهم.
2.2 المباني والمرافق
2.3 المعدات
2.4 إدارة المستندات
2.5 التصميم والتطوير
2.6 المشتريات
يجب على المُصنِّع وضع إجراءات رقابة على الشراء لضمان مطابقة جميع المنتجات والخدمات المشتراة أو المُستلَمة للمتطلبات المحددة، والتي لا تقل عن المتطلبات ذات الصلة بالقوانين الوطنية والمعايير الإلزامية. يجب أن تكون بيانات الشراء قابلة للتتبع.
يُقيِّم المُصنِّع ويختار الموردين والمقاولين والاستشاريين المُحتملين بناءً على قدرتهم على تلبية المتطلبات المحددة، بما في ذلك متطلبات الجودة. ويجب توثيق هذا التقييم.
2.7 إدارة الإنتاج
على المُصنِّع إنشاء نظام إدارة جودة لضمان استيفاء المنتج لمتطلبات المعايير الإلزامية والمتطلبات الفنية.
يُجمِّع المُصنِّع الإجراءات التكنولوجية، وإجراءات التشغيل القياسية، وما إلى ذلك لتحديد العمليات الرئيسية والإجراءات الخاصة.
يجب أن تكون جميع معلومات الإنتاج قابلة للتتبع.
2.8 مراقبة الجودة
2.9 خدمات المبيعات وما بعد البيع
2.10 مراقبة المنتجات غير المطابقة
2.11 مراقبة الأحداث السلبية وتحليلها وتحسينها
3. المشاكل الشائعة أثناء فحص GMP
- نقص الكوادر المؤهلة لإجراء مراجعات المواد المطلوبة واتخاذ قرارات التخلص؛
- نقص التدريب والتقييم للمناصب الخاصة؛
- عدم امتثال البيئة والمرافق؛ تصميم الدرجات – فرق الضغط غير معقول؛
- عدم توافق ملفات التصميم والتطوير مع ملف طلب التسجيل؛
- ارتباك في مراقبة المشتريات، وعدم وجود شهادة جودة للمواد الخام؛
- نقص في إجراءات إدارة المنتجات غير المطابقة
